Je fais une petite rediffusion d’une vieille note datant de 2010.
À l’époque, ce sont les déclarations du Pr, ci-dessous, qui avaient motivées la rédaction de cette note. Il n’avait pas aimé mon billet et s’était plaint au conseil de l’ordre. J’avais exagéré, je m’étais pas mal moqué, sans que cela apporte quoi que ce soit à la controverse. J’avais donc ré-écrit ce billet, en supprimant toute mention du Pr. Cette épisode a été une grande leçon dans ma carrière de blogueur. Pas besoin d’être méprisant quand on souhaite faire avancer le débat. Vous verrez, la note fait quelques allusions à l’actualité de l’époque. je n’ai rien changé pour la garder dans son jus, hormis corriger ou supprimer les liens obsolètes.
Juste une petite précision supplémentaire, pour un médicament à marge thérapeutique étroite, les bornes de la bioéquivalence sont de 90%-110%, et non pas de 80%-125%.
Bonne lecture 😉
°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°O°
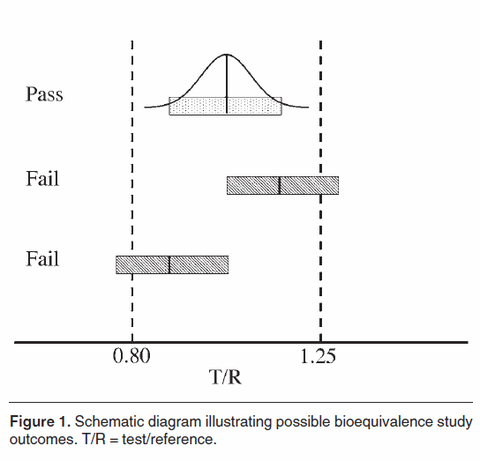
Un des principaux reproches fait par les adversaires des génériques est l’apparemment très large fourchette de tolérance (entre 80 et 125%) acceptée par les autorités sanitaires françaises lors de la détermination de la bioéquivalence d’un générique et d’un princeps.
Je n’ai jamais trouvé d’explications bien satisfaisantes sur ces limites. Pourquoi elles et pas d’autres ?
La plupart des documents sont soit non explicatifs, soit tellement techniques que je n’y comprends strictement rien.
Mais on va quand même essayer d’éclaircir un peu les choses.
Premièrement, ce n’est pas l‘action qui varie entre 80 et 125%, mais la biodisponibilité.
 Byers JP, Sarver JG. Pharmacokinetic Modeling. In Hacker M, Bachmann K, Messer W. Pharmacology Principles and Practice. London: Academic Press; 2009. p. 202.
Byers JP, Sarver JG. Pharmacokinetic Modeling. In Hacker M, Bachmann K, Messer W. Pharmacology Principles and Practice. London: Academic Press; 2009. p. 202.
Par exemple, pour le clopidogrel, si tant est que l’on puisse mesurer son action autrement que par des critères cliniques ce serait par un test d’agrégabilité plaquettaire. Sa biodisponibilité est mesurée notamment par l’aire sous la courbe (ASC en français, AUC en anglais) des concentrations plasmatiques de clopidogrel en fonction du temps (AUC 0-t).
La biodisponibilité est censée être un reflet de l’efficacité. Tout le système de la bioéquivalence repose sur cette approximation. Après, on peut s’écharper sans fin pour savoir quelle est l’exactitude de cette approximation. Je ne vais pas rentrer dans ce débat.
Deuxièmement, et cela me semble bien plus important, ces bornes sont des bornes maximales d’acceptabilité.
C’est à dire qu’elles ne reflètent pas du tout la différence de biodisponibilité effectivement constatée entre un générique et un princeps.
Je vais prendre un exemple « chaud », un essai de bioéquivalence entre le Plavix® et le clopidogrel Mylan® qui a permis à ce dernier d’obtenir une AMM européenne.
Ce princeps et ce générique contiennent des sels différents: chlorydrate pour le générique et hydrogène sulfate pour le princeps. Mais dans les deux cas, c’est bien la biodisponibilité du clopidogrel que l’on mesure (petit rappel sur le métabolisme du clopidogrel ici).
Cet essai est disponible ici, à partir de la page 10.
Je ne vais pas décrire le protocole qui est le même pour la plupart des essais de bioéquivalence. Ici, on a étudié 96 sujets sains.
Les résultats sont les suivants (page 12) et représentent la disponibilité du clopidogrel dans le plasma:
Comme ça, ça fait peur, mais en fait, ce n’est pas si compliqué que cela.
On va se contenter de regarder la première colonne, c’est à dire l’aire sous la courbe entre t0 et un instant t: AUC 0-t.
Test, c’est le générique, Reference le princeps.
Ratio, c’est le rapport entre l’aire sur la courbe du test sur celle de la référence. C’est ce ratio dont l’intervalle de confiance doit se situer entre 80% et 125%. Ici, ce ratio est de 100% avec un intervalle de confiance de 90-110% On est donc parfaitement au sein des bornes.
BM Davit et al. Ann. Pharmacother., Oct 2009; 43: 1583 – 1597.
On va regarder très rapidement les autres colonnes: les Cmax (la concentration maximale de clopidogrel), Tmax (le temps mis pour arriver à la Cmax), et la demi-vie sont sensiblement les mêmes pour le générique et le princeps.
Voici deux autres exemples de ratios observés pour AUC 0-t:
- clopidogrel Sandoz®: 90.43%
- clopidogrel Qualimed®: 100%
Maintenant, vous allez me dire que ce ne sont que 3 exemples.
J’en conviens parfaitement.
Mais il y a des gens qui ont regardé de près cette fameuse différence effective. Ils ont étudié 2070 essais de bioéquivalence déposés depuis 12 ans devant la FDA.
La différence moyenne observée entre les aires sous la courbe du princeps et du générique est de…3.56%.
Dans 98% des cas, cette différence était inférieure à 10%. Le résumé de cette étude publiée dans Annals of Pharmacotherapy est ici.
Un argument des adversaires des génériques souligne que l’aspect du générique peut troubler les patients. Mais je pense qu’un peu de pédagogie peut le plus souvent améliorer les choses.
Enfin, ils accusent parfois les autorités sanitaires de ne pas analyser les génériques avec la même rigueur que les princeps.
Le problème est que de nombreuses autorités sanitaires, et non des moindres (EMA, FDA, autorités sanitaires japonaises, australiennes, sud-africaines, canadiennes) utilisent grosso modo les mêmes limites 80-125 et les mêmes protocoles d’études de pharmacovigilance.
Admettons que l’Afssaps (qui suit les protocoles de l’EMA, mais admettons quand même) soit aux ordres de Roselyne qui veut faire des économies à tout prix sur le dos des patients, j’arrive plus difficilement à comprendre que notre brillante Ministre ait une telle influence au niveau mondial. Dans le même ordre d’idées, j’ai du mal à imaginer une telle unanimité autour de protocoles qui seraient si peu rigoureux.
Peut-être un complot mondial concocté par un groupe de génériqueurs qui tire les ficelles du fond de leur base secrète édifiée sous le volcan Eyjafjöll ?
(c’est en réalisant un essai clinique de bioéquivalence de l’ExforgeHCT® qu’ils auraient accidentellement provoqué la fameuse éruption)
Je n’y crois pas trop.
°0°0°0°0°0°0°0°0°0°0°0°0°0°
CPMP. Note for Guidance on the Investigation of Bioavailability and Bioequivalence.
CHMP. Guideline on the Investigation of Bioequivalence.
Barbara M Davit, Patrick E Nwakama, Gary J Buehler, Dale P Conner, Sam H Haidar, Devvrat T Patel, Yongsheng Yang, Lawrence X Yu, and Janet Woodcock. Comparing Generic and Innovator Drugs: A Review of 12 Years of Bioequivalence Data from the United States Food and Drug Administration. Ann. Pharmacother., Oct 2009; 43: 1583 – 1597.
Rapport du CNOM sur le médicament générique, 4 février 2010.



Concernant le pourquoi des bornes 80 et 125%, il semble que ce soit une histoire de logarithme !
L’utilisation des tests statistiques est facilitée lorsque la variable étudiée suit une loi proche d’une loi normale. La littérature scientifique indique que, comme d’autres paramètres biologiques, les variables AUC et Cmax ne suivent pas une loi Normale mais sont plus proches d’une loi « log normale ».
Afin de « normaliser » la distribution, les variables recueillies lors de l’essai clinique de bioéquivalence sont transformées en leurs logarithme naturel . Il en va de même pour les bornes de l’intervalle de confiance .
Les agences du médicaments considèrent que la bioéquivalence est admise lorsque la biodisponibilité moyenne du générique mesurée par l’AUC et/ou Cmax n’excède pas plus ou moins 20% de la biodisponibilité du médicament test.
En retenant les valeurs limites non transformées de 80% et 125 % on obtient en valeurs log transformées :
Ln 0,8 =-0,223 et Ln1,25= +0,223. Ce qui à l’avantage de correspondre à un intervalle symétrique. Une fois l’analyse statistique faite , on retrouve les résultats à l’échelle non-transformée en calculant les exponentielles des valeurs obtenues .
Excellent, merci!
les mutuelles remboursent moins cher, est-ce que leurs cotisations baissent?
Je me suis toujours demandé pourquoi un générique devait aux yeux des anti-génériques faire moins bien que le princeps. S’il peut faire « différen » ne peut il faire mieux ?
Quant à l’affaire du Lévothyrox®: étrange.
Les doses de levothyroxine sont ajustables à 12,5 microgrammes près. Le plus petit comprimé de 25 microgrammes étant sécable en 2.
Or les posologies moyennes sont de 1,7 µg/kg/jour pour les traitements substitutifs et de 2,1 à 2,5 µg/kg/jour pour les traitements freinateurs (Vidal® dixit) .
Donc personne n’est équilibré « au poil près » d’autant que les besoins varient d’un jour à l’autre.
Admettons qu’il y ait une toute petite variation d’absorption par rapport à la composition antérieure. C’est probablement moins que 12,5 microgrammes par jour de différence.
On comprend mal des signes majeurs rapportés aux nouveaux excipients , que l’on ne rencontre même pas dans grand nombre d’hypo- ou hyperthyroïdie bien frappées si je puis dire .
De plus certains des signes rapportés à la radio (« dans le poste ») ne sont pas des signes classiques d’hypo- ou hyperthyroïdie.
Alors parmi les hypothèses scientifiques on a, il me semble :
de toutes petites différences de taux de LT4 peuvent avoir des effets majeurs. Comme une hypo ou hyperthyroidie massive . Ca existe ? Je ne sais pas, pas mon domaine.
on a empoisonné les comprimés de certains lots. Ou il y a introduction accidentelle de produit toxique. Reste que les effets du poison sont très variés, ce qui est peu logique.
les nouveaux excipients , acide citrique, mannitol, ont des effets secondaires très variés. A creuser.
de très nombreux patients sont traités. Forcément, parmi ces 3 millions de patients des événements pathologiques indépendants vont se produire chez certains et coïncider. Début d’une polyarthrite rhumatoïde, fracture de jambe, méningite virale, constipation, diarrhée, pâleur, rougeur , urticaire, syphilis, mal de tête , de muscle, d’articulation, de tendon, de ventre de thorax… etc
Lorsqu’aucune cause n’est apparente on va incriminer le nouveau comprimé. La multiplication des cas peut, je dis peut, être le fait de la suggestion + le hasard des coïncidences. Homo sapiens a tendance à faire le lien de causalité un peu imprudemment, et depuis la nuit des temps. Les phénomènes de réactions de stress collectives sont une réalité médicale qu’il faut bien évoquer, au prix de l’incorrectitude politique , au risque de choquer mais ce n’est pas une insulte c’est un diagnostic possible.
J’oublie peut – être quelque chose… je sais pas tout…
Bonjour,
Je précise que pour une même spécialité, l’intervalle 80-125 ou 90-110 ou 90-105 (cas de la lévothyroxine) selon la spécialité doit être respecté. Les génériques disposants de formulations plus performantes, il n’est pas rare de constater que pour une spécialité générique la dispersion gaussienne soit plus étroite que pour la spécialité de référence. Ce qui de fait tord le cou aux idées reçues dénonçant des variations (très faibles en plus) dans les études de bio-équivalence, sans préciser que le princeps lui même, entre deux lots va parfois varier davantage !
Rémi, pharmacien