Nicolas Sarkozy a chargé fin décembre le député UMP et chirugien Bernard Debré de rédiger un rapport sur l’affaire du Mediator, selon France Info. Le rapport, qui devrait inspirer une loi, sera remis en mars au chef de l’État et au ministre de la Santé, Xavier Bertrand, précise la radio.
Bernard Debré y préconisera que l’Agence française de sécurité sanitaire des produits de santé (Afssaps) soit financée directement par l’État et non par l’industrie pharmaceutique, et proposera également de rendre publique la liste des contrats qui lient les professeurs de médecine à des laboratoires pharmaceutiques.
Lu sur lci.fr ce matin.
Une question et une remarque.
La question: comment connait-on le contenu d’un rapport un peu plus de 1 mois avant qu’il soit remis officiellement? Si le rapporteur l’a déjà écrit, pourquoi ne pas le remettre maintenant? Cela implique aussi que l’affaire du Mediator® est close, que tout est connu et rien de nouveau va être connu, par exemple entre maintenant et mars…
La remarque: cela fait pas mal d’années que les experts des agences et des sociétés savantes, entre autres les PU-PH remplissent consciencieusement leur déclaration de conflit d’intérêt. Certes, on ne connait ni les montants ni la nature des contrats, mais on connait l’existence de liens. Est-ce que cela a empêché les vilains doutes de collusion dans l’affaire du Mediator®? Est-ce que, actuellement, ces déclarations permettent sereinement au lecteur d’un avis de l’Afssaps/HAS ou d’une recommandation de l’ESC de faire confiance à un texte écrit par des auteurs qui ont un lien financier avec les firmes pharmaceutiques qui commercialisent un produit concerné par cette recommandation/avis?
Mais le problème réside aussi ailleurs.
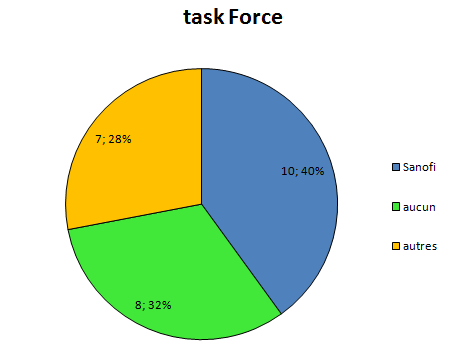
Faites-vous donc confiance aux dernières recommandations de l’ESC sur la place donnée à la dronédarone, commercialisée et développée par Sanofi, dans la prise en charge de la fibrillation auriculaire, en sachant que 40% des rédacteurs ont un lien financier avec cette firme?
Bon, la question et la réponse ont peu d’importance.
En effet, ces recommandations guident non seulement notre pratique courante, mais aussi peuvent potentiellement servir de base médico-légale.
Vous êtes dubitatifs devant ces recommandations. Vous débutez chez un patient sans cardiopathie un traitement par amiodarone/sotalol/flécaïnide. Le patient présente un effet secondaire sévère. Lui ou sa famille vous cherchent des noises en vous collant sous le nez (ou celui d’un juge) ces recommandations où la dronédarone passe avant l’amiodarone et les autres anti-arythmiques.
Comment allez-vous vous justifier? En dégainant le magazine Prescrire et votre quête d’indépendance en face de recommandations européennes (et incidemment américaines)?
Cette situation est un peu caricaturale car étant donné les doutes actuels sur la sécurité du produit, et la réévaluation en cours de sa balance bénéfices/risques par l’EMA, vous ne risquez probablement rien.
Mais cela sous-entend qu’il est nécessaire d’aller au delà de la déclaration des conflits d’intérêts dans les sociétés savantes ou les agences de régulation, il faut qu’il n’y en ait plus.

mode avocat du diable : D’un n’autre coté il ne faudrait pas non plus que les experts soient de gens n’ayant aucune idée de la facon dont les labo fonctionnent.
Cela dit le problème me semble plus fondamental que ca:
Si les labos produisaient des molécules efficaces plus souvent, ils n’auaient pas à dépenser des sommes énormes pour vendre leurs molécules peu efficaces.
J’ai tout de même peine à croire qu’il est moins risqué pour une entreprise de faire de la pub en masse pour vendre de la daube plutôt que d’invertir (certes avec de gros risques également) pour tenter de produire un truc qui marche.
@Xavier au dessus
Le souci, c’est que le marketing, on est sûr que ça marche, hélas, la recherche, c’est moins déterministe…
Sous réserve d’un avis juridique éclairé, il me semble que les recommandations ne sont pas opposables.
En revanche, le RCP du médicament de même que la notice sont vraiment de nature à être une référence en cas de litige, que ce soit pour le non respect des indications, d’une contre-indication ou des précautions d’emploi en cas de problème…
C’est bien le RCP qui définit quelle est la circonstance de prescription d’un médicament et les inconvénients potentiels.
Opposer les recommandations européennes serait curieux et tu peux toujours opposer la fiche de transparence française: ASMR de niveau V par rapport à l’AMIODARONE… Dans cette matière, on peut trouver tout et son contraire… si on cherche bien. Ce qui compte le plus je pense c’est d’être attentif au RCP et de le respecter. Ce document est incontournable en cas de contestation.
Pour la DRONEDARONE si elle continue dès son début de carrière à exploser le foie des patients, je doute que cette carrière soit très longue mais peut-être que le labo aura récupéré un peu sa mise? Gagner du temps… C’est peut être le deal des médicaments douteux vites mis sur le marché et retirés plus ou moins rapidement quand la vraie vie finit d’achever leur balance bénéfice risque.
Sur la question de l’indépendance, je pense que la revue Prescrire est un bon exemple de ce qu’une expertise peut se construire sans aucun lien d’intérêt avec les firmes. Il faut se donner les moyens de développer ce type d’expertise, impliquer les praticiens de terrain plus proches « de la vraie vie » dans les choix thérapeutiques finaux et écarter les représentants des firmes. L’expertise pour la pratique clinique doit être conduite sans aucun lien avec l’industrie. Bien sûr ce type d’expertise nécessite d’y être formée et de la rigueur mais n’exige absolument pas de travailler pour les firmes.
Tu as raison, j’avais totalement oublié l’avis peu favorable de la HAS!
Pour l’opposabilité, je serais en effet assez curieux d’avoir un avis juridique…
un médecin a été condamné en cassation (http://www.courdecassation.fr/publications_cour_26/arrets_publies_2986/premiere_chambre_civile_3169/2010_3318/octobre_3686/888_14_17835.html) sur quelles références ? une lettre de pharmacovigilance du laboratoire, une recommandation de l’afssaps et un article de Prescrire. Donc, oui, en théorie une recommandation n’est pas opposable, mais il faut apporter des biscuits, et des bons, avant de s’opposer à une recommandation. Dans l’affaire de la Dronedarone, à partir où le laboratoire a fait une lettre d’alerte (tout comme la warning box du Clopidogrel … qui vient de Sanofi aussi, tiens tiens, le service juridique de Sanofi est trop fort pour se prémunir des coups futurs qui pourraient leur retomber dessus), le médecin prescripteur est tout à fait en droit (devoir) d’aller contre les recommandations si un élément nouveau est arrivé depuis les recommandations
Terrible, cette histoire…
Bon, ni âge ni poids sur la prescription d’un enfant, ce n’est pas bien du tout….
Ce cas est intéressant pour l’erreur de dispensation (Catalgine°) et montre qu’être pointilleux sur la rédaction d’une ordonnance n’est probablement pas une mauvaise idée.
Pour reprendre un exemple auquel je tiens:
FLUINDIONE 20 MG Comprimé (Previscan°): 15 mg (3/4) le soir
en précisant au niveau de l’identification du patient avec la taille, le poids et la clairance de la créatininémie: la cible INR.
Prescrire une dose et rappeler la cible INR sur l’ordonnance.
LA (seule) réponse standard de l’Afssaps est beaucoup plus simpliste pour éviter les erreurs qui d’ailleurs se répètent et conduisent aux mêmes rappels aux professionnels de santé (« vérifier et être vigilant »…). (cf. lettres aux prescripteurs PREVISCAN et PRESERVISION, LAMISIL et LAMICTAL etc). L’Afssaps oublie d’ailleurs de rappeler la loi pour LAMISIL et LAMICTAL puisque la prescription en DCI est OBLIGATOIRE pour ces deux substances et ne l’indique absolument pas dans son texte en mettant en avant les noms de fantaisie! J’attends toujours la réponse de l’Afssaps sur ce sujet!!! Le « gendarme » du médicament ne doit-il pas rappeler la loi aux différents acteurs?
Je ne comprend pas cet engouement pour tout ce qui est nouveau. On a des traitements qu’on utilise depuis longtemps, qui sont efficaces et éprouvés, qu’on sait surveiller.
Il arrive un truc nouveau et hop, on le recommande. On n’a aucun recul mais c’est pas grave! C’est pas comme si on risquait la santé et la vie des patients…
Ben, le marketing nous assène depuis des années que médicament innovant=progrès…
Or, ce n’est pas forcément le cas.